摘要: 采用熔融冷却法制备了Na2O-CaO-La2O3-B2O3-SiO2玻璃,经热处理获得了硅酸盐氧基磷灰石硼硅酸盐玻璃陶瓷,并采用X射线衍射(XRD)、傅里叶变换红外光谱(FTIR)、差示扫描量热法(DSC)、产品一致性试验(PCT)法等方法探究了CaO取代SiO2对该硼硅酸盐玻璃陶瓷物相、微观结构和化学稳定性的影响规律。结果显示:随着CaO含量增加,硅酸盐氧基磷灰石晶相衍射峰增强,其他晶相的衍射峰减弱直至消失,当CaO摩尔分数为15%时获得只含CaLa4(SiO4)3O晶相的玻璃陶瓷样品;CaO含量会对玻璃陶瓷的晶相种类和晶体形状、大小、分布产生影响,CaO含量变化会造成陶瓷相晶体发生团簇和长大;采用PCT法浸泡28 d后,所有样品关于Si、Ca、La三种元素的归一化浸出率(g·m-2·d-1)均保持在10-3数量级以下,表明其具有优异的化学稳定性,且CaO摩尔分数为15%的玻璃陶瓷样品化学稳定性最优异。研究结果表明,硅酸盐氧基磷灰石硼硅酸盐玻璃陶瓷是固化富La和某些锕系元素高放废物的潜在基材。
关键词: CaO, 硼硅酸盐玻璃陶瓷, 硅酸盐氧基磷灰石, 晶相, 浸出率, 化学稳定性
0 引 言
乏燃料后处理必然会产生高水平放射性废物(简称:高放废物),这些高放废物不仅具有高放射性,还含有锕系元素、镧系元素等重金属元素,直接将其排放会严重危害环境。目前国际社会广泛接受处理高放废物的方法为:先使用惰性基材将其固化处理,再进行深地质填埋,以达到与生物圈隔绝,防止高放废物危害环境[1]。玻璃固化是目前唯一具有工业化应用的固化方法,其中硼硅酸盐玻璃应用最广泛、固化效果最优异[2]。然而高放废物中的硫、氯、重金属元素等在玻璃基材中易引发分相[3],导致其在玻璃基材中的溶解度低,造成废物包容量低、固化体稳定性差等问题[4]。
玻璃陶瓷固化是通过在玻璃中形成稳定微晶相,可将高放废物中长寿命核素或难溶组分固化进入稳定的微晶相晶格,剩余组分溶解于玻璃相,形成玻璃陶瓷固化体,其废物包容量和稳定性通常较同组分的玻璃固化体优异,兼具玻璃固化包容元素多和陶瓷固化稳定性高等优点[5-6],被认为是最具潜力的固化方式之一,可用于“难溶”高放废物的固化处理[7]。对于玻璃陶瓷固化体,常见晶相有钙钛锆石、烧绿石、钼钨钙矿、硅酸盐氧基磷灰石、独居石等[8-12]。富硅酸盐氧基磷灰石(A,AE)2RE8 (SiO4)6O2 (A 为碱金属元素,AE 为碱土金属元素,RE 为稀土元素)的玻璃陶瓷固化体化学稳定性十分优异,能对镧系和锕系元素含量较高的高放废物进行固化[13-15]。Peterson 等[14] 采用传统冷压烧结法制备了氧基磷灰石(Ca2Nd8 (SiO4)6O2),并在90 ℃的条件下对制得的氧基磷灰石样品进行了 5 d 的浸出实验,最终测得 5 d 时间里 Ca 的归一化损失大约为0. 024 g·m- 2,表明氧基磷灰石具有优异的化学稳定性。Ravikumar 等[16] 研究了放射性核素离子取代对硅酸盐氧基磷灰石 CaLa4(SiO4)3O 热膨胀行为的影响,表明氧基磷灰石具有各向异性热膨胀的特征,且氧基磷灰石具有较好的热稳定性。以上研究表明,硅酸盐氧基磷灰石具有优异的化学稳定性、热稳定性,使其成为放射性元素的宿主相提供了有力的保障。余宏福等[11]以铈(Ce)、钕(Nd)模拟锕系元素,通过固定配方中Ce 的含量,逐渐增加 Nd 的含量,制备出了可以同时固化 Ce 和 Nd 且化学稳定性优异的铈钕-硅酸盐氧基磷灰石玻璃陶瓷。目前,关于氧基磷灰石玻璃陶瓷固化的研究主要集中在以 Ce 或 Nd 模拟锕系元素,探究氧基磷灰石对高放废物中锕系元素的固化特性[17]。然而,对于含有大量镧(La)元素的高放废液[18]而言,由于Ce 和 Nd 的离子半径与 La 的离子半径存在差异,因此以 Ce 和 Nd 作为模拟元素则不能完全反映 La 在氧基磷灰石玻璃陶瓷中的赋存状态,且 La 元素可以用于模拟部分锕系元素[19],以研究其对形成的玻璃陶瓷固化体的物相、结构和性能的影响规律。 基于此,研究富含 La 的氧基磷灰石相-硼硅酸盐玻璃陶瓷为氧基磷灰石相玻璃陶瓷固化的研究提供了新的思路。
CaO 作为玻璃网络修饰体,在硼硅酸盐玻璃网络结构起解聚玻璃网络连接的作用,进而影响硼硅酸盐玻璃的析晶行为。此外,Ca2+也是氧基磷灰石相的主要成分之一,其含量直接影响硅酸盐氧基磷灰石晶体的结构。目前,CaO 对镧硼硅酸盐玻璃陶瓷晶相的影响研究主要集中在 CaO 取代 Na2O 对镧硼硅酸盐玻璃陶瓷晶相的影响方面,如 Quintas 等[20]研究了富稀土铝硼硅酸盐玻璃的结晶行为与 R(R = CaO/ (Na2O + CaO))的关系,发现增大组分中 CaO 的含量会形成 Ca2+xNd8-x(SiO4)6O2-0.5x(x≈0. 4 ~ 0. 7)硅酸盐磷灰石相,且在对含镧玻璃系列的平行研究中也发现了相同的规律。然而,硅酸盐氧基磷灰石晶体中含有[SiO4]四面体基团,SiO2 含量变化必定与氧基磷灰石的析晶存在关联。因此,研究 CaO 取代 SiO2 对硅酸盐氧基磷灰石玻璃陶瓷的析晶影响非常必要,这在一定程度上丰富了 CaO 对氧基磷灰石析晶影响的研究内容,为后续有关氧基磷灰石析晶的研究提供了一定的参考意义。
基于以上论述,本研究以简化的含 La 和 Ca 的 Na2O-CaO-La2O3-B2O3-SiO2 硼硅酸盐玻璃为基础玻璃,采用二次热处理的方法制备氧基磷灰石相玻璃陶瓷,并探究 CaO 取代 SiO2 对该镧硼硅酸盐玻璃陶瓷析晶性能、结构及其化学稳定性的影响规律。
1 实 验
1. 1 样品制备
以 9Na2O-xCaO-9La2O3-15B2O3-(67 - x)SiO2 为基础玻璃,其中 x = 3、6、9、12、15 和 18,用分析纯 SiO2(≥99. 0% ,质量分数,下同)、H3BO3 (≥99. 5% )、Na2CO3 (≥99. 8% )、CaCO3 (≥98. 5% )、La2O3 (≥98. 0% )为原料,样品名称及具体化学组成见表 1。然后将制备的玻璃进行二次热处理获得玻璃陶瓷样品。其详细制备过程为:按表 1 中的配方分别称取 20 g 原料,在玛瑙研钵中充分混合均匀获得配合料;将配合料置于 50mL 刚玉坩埚中,于高温炉中升温至600 ℃保温2 h 以去除 H2O 和 CO2 ,再继续升温至1 300 ℃保温2 h,得到均匀玻璃熔体,浇注到预热好的石墨板上急冷获得基础玻璃;将获得的基础玻璃以 5 ℃ / min 的升温速率从室温升温至晶化温度保温 2 h 使玻璃样品充分析晶,自然冷却至室温,获得玻璃陶瓷样品。
表 1 不同 CaO 含量样品的化学组成

1. 2 样品结构及性能表征
样品的体积密度采用全自动固体密度计(型号:ST-600A)测量,其密度精度为 0. 001 g/cm³。在室温下,选用粉末样品,采取阿基米德排水法测量样品的实际密度,计算公式如式(1)所示。

式中:ρ 为样品实际密度,g/cm³;m1 为装有约 1/3 样品粉末的比重瓶质量与干燥的空比重瓶质量的差值,g;m² 为装有约 1/3 样品粉末的比重瓶装满脱气蒸馏水的质量,g;m³ 为比重瓶未装样品粉末但装满脱气蒸馏水的质量,g;ρ1 为实验温度下脱气蒸馏水的密度值,g/cm³。
差示扫描量热法数据通过同步热分析仪(型号:NETZSCH-STA 449F5) 采集,取大约 10 mg 粒径小于75 μm 的样品粉末,在 N2 气氛下以 20 ℃ / min 的升温速率升温到 1 000 ℃ 。X 射线衍射谱使用 Cu-Kα 辐射的 X 射线衍射仪(型号:Rigaku-DMAX1400)测试,在 40 kV 和 40 mA 的工作条件下于 2θ = 10° ~ 80°范围内工作,获取步长为 0. 02°,扫描速度为 20 (°) / min。傅里叶变换红外光谱(400 ~ 2 000 cm-1)是通过标准 KBr粉末压片法制样,使用傅里叶变换红外光谱仪进行测定。使用扫描电子显微镜(型号:Hitachi-TM4000)观察样品的微观形貌,将表面平整的薄片玻璃陶瓷样品在质量分数为 5% 的氢氟酸中腐蚀 60 s,然后洗涤干燥,进行喷金后对样品进行微观形貌观察。同时,扫描电子显微镜配备了能量色散 X 射线探测器。
化学稳定性的评估方法是产品一致性试验(product consistency test, PCT)法。将1 g 粒径在75 ~ 150 μm的样品粉放入聚四氟乙烯容器中,加入 10 mL 超纯水进行浸泡,并将容器密封。然后将聚四氟乙烯容器放入反应釜中密封并静置于(90 ± 1) ℃恒温装置中,分别于 1 d、3 d、7 d、14 d 和 28 d 时取出浸出液。使用电感耦合等离子体发射光谱仪(型号:ICAP6500) 测定浸出液中相关元素的浓度。各元素归一化元素浸出率(LRi,g·m-2·d-1)的计算公式如式(2)所示。

式中:Ci 为元素 i 在浸出液中的浓度,mg·L-1;fi 为元素在样品配方中的质量分数;Δt 为浸出时间,d;V 为浸出液体积,L;S 为样品的表面积,m²。当选用1 g 粒径在75 ~ 150 μm 的样品粉末,浸出液为10 mL 时,S/V 的值为 2 000 m-1。
2 结果与讨论
2. 1 玻璃样品 XRD 和 DSC 分析
图 1 是不同 CaO 含量基础玻璃样品的 XRD 谱。 由图可知,当 CaO 摩尔分数小于等于 15% 时,XRD 谱中只观察到了非晶态的馒头峰,样品呈现完全非晶的特征;当 CaO 摩尔分数为 18% 时,XRD 谱中出现了Ca3La6 (SiO4)6 的衍射峰,表明通过熔融冷却法获得的基础玻璃样品发生析晶。 由于 Ca3La6 (SiO4)6 晶相的析出会影响其他含钙硅晶相的生成[21],所以在进行热处理制备玻璃陶瓷时,选择 CaO 摩尔分数小于等于15% 的基础玻璃样品。
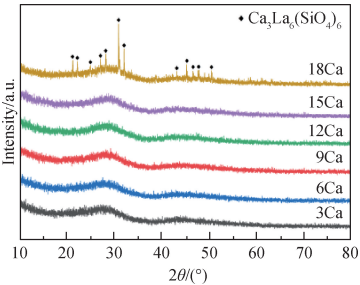
图 1 不同 CaO 含量玻璃样品的 XRD 谱
图 2 为不同 CaO 含量基础玻璃样品的 DSC 曲线。每条 DSC 曲线在 500 ~ 700 ℃ 有一个吸热峰,在700 ~ 900 ℃有一个放热峰。一般而言,吸热峰的初始温度为玻璃化转变温度(Tg),其值与玻璃化结构调整密切相关,放热峰的峰值温度为析晶温度(Tp)[22]。由图 2 可知,随着 CaO 含量增加,Tg 逐渐降低。这是由于随着 CaO 含量增加,玻璃组分中的游离氧含量增加,起着解聚玻璃网络结构的作用,因而 Tg 值降低。所有玻璃样品的 DSC 曲线都有一个较大的放热峰,说明样品易于析晶,可获得析晶良好的玻璃陶瓷材料[23]。通常,玻璃的实际析晶温度比 DSC 测得的 Tp 值高 50 ~ 100 ℃[24],因此本研究二次热处理制备玻璃陶瓷样品时选用的晶化温度为 900 ℃ 。
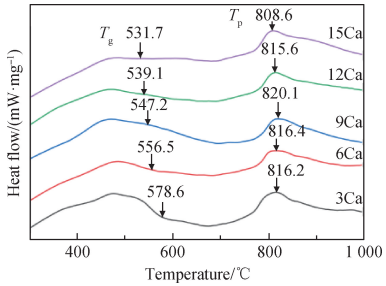
图 2 不同 CaO 含量玻璃样品的 DSC 曲线
2. 2 玻璃陶瓷样品 XRD 分析
图3 是不同 CaO 含量玻璃陶瓷样品的 XRD 谱。由图可知,将基础玻璃在 900 ℃进行热处理后,都制得了玻璃陶瓷样品。当玻璃陶瓷样品中 CaO 摩尔分数为 3% 和6%时,可以检测到 NaLa9(SiO4)6O2 (PDF No. 32-1109)、LaBO3 (PDF No. 13-0571)、Na2Si2O5 (PDF No. 19-1236)和 Na2B4O7 ( PDF No. 51-1716 ) 等晶相的衍射峰;当 CaO 摩尔分数为 9% 时, XRD谱中开始出现了CaLa4(SiO4)3O(PDF No. 71-1368)的衍射峰;当 CaO 摩尔分数为12% 时,CaLa4(SiO4)3O 的 XRD 衍射峰强度进一步增强,LaBO3 、Na2Si2O5 和 Na2B4O7 等杂相的衍射峰强度减弱,而 NaLa9(SiO4)6O2 的衍射峰消失;当CaO摩尔分数达到 15% 时, XRD 谱中只存在CaLa4(SiO4)3O 的衍射峰。由 XRD 结果可知,玻璃陶瓷样品主晶相的晶体结构为硅酸盐氧基磷灰石[25-26],仅硅酸盐氧基磷灰石晶体种类发生了改变。当 CaO 摩尔分数低于 9% 时,硅酸盐氧基磷灰石晶体以 NaLa9(SiO4)6O2 的形式析出;当 CaO 摩尔分数达到 9% 后,继续增加 CaO 含量,则是析出 CaLa4(SiO4)3O。随着 CaO 含量的增加,Ca2+ 对 NaLa9(SiO4)6O2 中 Na+ 和 La3+所占据的位点进行了等量取代,发生类质同晶的取代现象,形成了 CaLa4 ( SiO4 )3O。在 XRD 谱中,当 2θ在 30° ~ 31°时,随着 CaO 摩尔分数从 3% 增加到 15% ,衍射峰的位置略微向大角度发生偏移。此外,rCa2+ (0. 112 nm)[27]小于 rLa3+ (0. 121 6 nm)[28]和 rNa+ (0. 106 nm)[29]的平均值,理论上析出的硅酸盐氧基磷灰石晶体晶格体积减小,这使得衍射峰的位置向高角度偏移。不仅如此,随着 CaO 含量增加,玻璃陶瓷样品中的 LaBO3 、Na2Si2O5 和 Na2B4O7 的衍射峰强度逐渐减弱直至消失,硅酸盐氧基磷灰石晶体的衍射峰强度逐渐增强。由此可见,增大 CaO 含量不仅可以促进硅酸盐氧基磷灰石晶体的析出,还可以抑制其他晶相的析出。
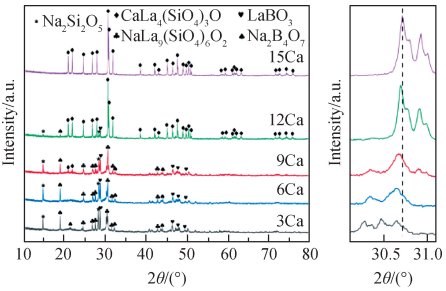
图 3 不同 CaO 含量玻璃陶瓷样品的 XRD 谱
使用 Jade6. 5 对玻璃陶瓷样品进行分析,并计算结晶度,结晶度计算公式如式(3)所示[30]。

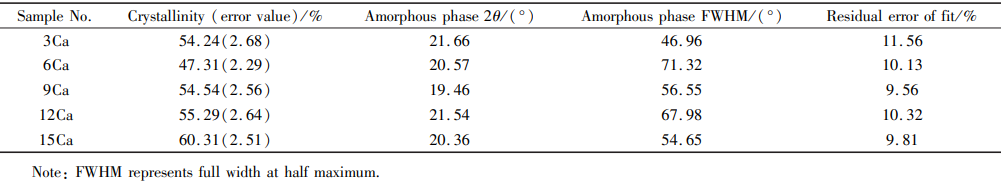
式中:X 为样品的结晶度;∑Ic 为晶体总衍射强度;∑Ia 为非晶部分的散射积分强度。得到的结晶度结果如表 2 所示。通过计算结果可知,随着 CaO 含量增加,玻璃陶瓷样品的结晶度总体上呈增大趋势。
表 2 不同 CaO 含量玻璃陶瓷的结晶度及其主要影响因素
2. 3 玻璃陶瓷样品 FTIR 分析
不同 CaO 含量玻璃陶瓷样品的 FTIR 谱如图 4 所示。样品的主要红外吸收峰在 400 ~ 2 000 cm-1,473 cm-1和 492 cm-1处的峰为网络结构或陶瓷相中[SiO4] 四面体的 Si—O—Si 键的弯曲振动峰[11,31];697 cm-1和 1 413 cm-1处的峰分别为 [BO3] 结构中B—O—B 的弯曲振动峰和[BO3 ]结构中B—O—B 拉伸振动峰[32];863 cm-1处的峰与[BO4]单元中 B—O 伸缩振动有关[2];1 043 cm-1附近的宽峰与玻璃网络结构和氧基磷灰石中[SiO4]四面体的 Si—O—Si 不对称振动有关[11];1 630 cm-1处的峰值与 H—O—H 键的弯曲拉伸模式有关[32]。
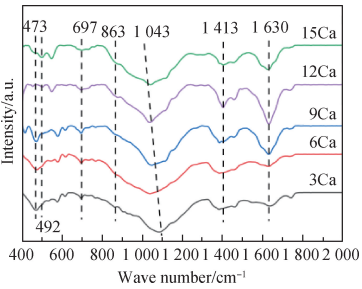
图 4 不同 CaO 含量玻璃陶瓷样品的 FTIR 谱
样品在473 cm-1和492 cm-1处的吸收峰是因为玻璃结构和陶瓷相中存在[SiO4]四面体[11],硅酸盐氧基磷灰石结构中存在[SiO4]四面体,结合 XRD 谱,进一步证实陶瓷相中存在硅酸盐氧基磷灰石晶相。随着CaO 含量增加,492 cm-1处的峰增强,这也与 XRD 谱反映的硅酸盐氧基磷灰石衍射峰随 CaO 含量增加而增强的结果一致。697 cm-1和 1 413 cm-1处的峰先变弱后增强,863 cm-1处的峰先增强后减弱,这是由于 CaO含量增加,玻璃结构中游离氧增多,从而促进[BO3]转换成[BO4],强化了玻璃结构,当 CaO 摩尔分数超过9% 时,过多的游离氧则会与玻璃网络结构中的[BO4]连接形成非桥氧,起到解聚作用。因此,结合 XRD 和FTIR 结果可知,当 CaO 摩尔分数低于 9% 时,[BO3]转换成[BO4],强化了玻璃结构,不利于析晶;当 CaO 摩尔分数大于 9% 时,[BO4]转换成[BO3],玻璃网络结构解聚,离子迁移更加容易,从而增大析晶的可能性,硅酸盐氧基磷灰石相强度较高。 1 043 cm-1处的峰随着 CaO 含量的增加逐渐向低波数偏移,这是因为配方中CaO 取代 SiO2 的量增大,使玻璃结构中的 Si—O—Si 总量减少[31]。
2. 4 玻璃陶瓷样品密度和 SEM 分析
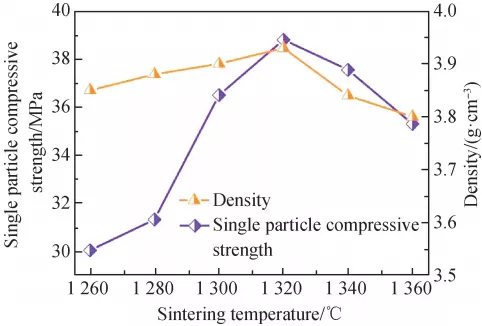
图 5 是不同 CaO 含量玻璃陶瓷样品的体积密度和摩尔体积变化图。CaO 含量增大,样品的体积密度呈增大趋势,摩尔体积为减小趋势。随着 CaO 含量增加,虽然玻璃网络结构发生解聚,解聚区增大,但 CaO 增多的同时引入了大量 Ca2+ 对解聚区起着填充的作用,这使得样品玻璃结构变得致密[5],同时基础玻璃发生析晶后,原子在晶体中的排布比在玻璃结构中更加有序且紧密,这些都会导致玻璃陶瓷样品摩尔体积减小,体积密度增大。图 6 为不同 CaO 含量玻璃陶瓷样品的实际密度和相对密度变化,选用 4 ℃ 时的水(ρ = 1 g/cm³)为参考物质计算相对密度。随着 CaO 含量增加,样品的实际密度呈减小趋势,这是由于 CaO的分子质量小于 SiO2 的分子质量造成的。结合样品体积密度和实际密度的变化趋势,可以得知,随着 CaO含量增加,玻璃陶瓷固化体越来越致密。
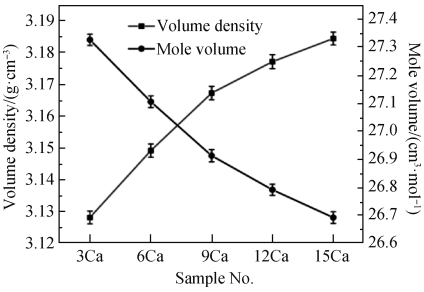
图 5 不同 CaO 含量玻璃陶瓷样品的体积密度和摩尔体积
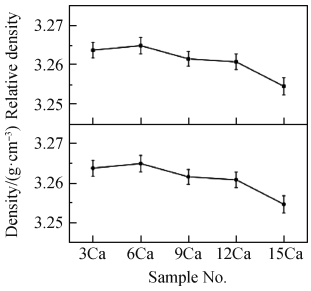
图 6 不同 CaO 含量玻璃陶瓷样品的实际密度和相对密度
图 7 为不同 CaO 含量玻璃陶瓷样品的 SEM 照片及 15Ca 样品关于 La 的元素分布图。所有样品均存在尺寸较小且分布较密的晶体[13,33-34]。结合样品密度结果可知,制得玻璃陶瓷样品内部结构致密。当 CaO 摩尔分数为 3% 时,样品析出粒状晶体,晶体尺寸极小,晶体相互堆叠在一起,分布不太均匀,存在微小间隙。当 CaO 摩尔分数为 6% 时,由图 7(b)可知,样品析出的晶体出现明显团聚现象,并观察到晶粒尺寸较大的短柱状晶体,这可能是团聚现象产生了局部空间,部分粒状晶体长大便形成了少量短柱状晶体。当 CaO 摩尔分数为 9% 时,由图 7(c)可知,样品团聚现象减弱,晶体为粒状,团簇减弱的原因与硅酸盐氧基磷灰石相强度的增强有关,短柱状晶体消失,这是团簇现象减弱造成的。当 CaO 摩尔分数为 12% 时,由图 7(d)可知,样品出现少量针状晶体[35],这与硅酸盐氧基磷灰石晶体发生的晶体种类改变有关。当 CaO 摩尔分数为 15%时,样品出现晶体分布均匀且晶体尺寸较小的粒状硅酸盐氧基磷灰石晶体。通过 SEM 可知,CaO 含量会影响镧硼硅酸盐玻璃陶瓷的陶瓷相晶体的大小、分布和形状[36]。由图 7(f)可知,La 元素在玻璃相和氧基磷灰石晶相中均呈现均匀分布,说明在晶化后,La 元素未全部进入氧基磷灰石晶相中,玻璃相中仍存在 La 元素。La 元素在两相中的均匀分布也说明了玻璃相和氧基磷灰石晶相均对 La 元素有良好的固化效果。

图 7 不同 CaO 含量玻璃陶瓷样品的 SEM 照片及 15Ca 样品关于 La 的元素分布图
2. 5 玻璃陶瓷样品化学稳定性分析
玻璃陶瓷样品关于 Si、Ca 和 La 的归一化浸出率(LRSi、LRCa和 LRLa)的计算结果如图 8 所示。结果表明,随着浸出时间的增加,样品的 LRSi、LRCa和 LRLa均呈现下降趋势,前 7 d 各元素的浸出率快速下降,7 d 后下降速度减缓,14 d 后浸出率下降幅度很小,基本保持不变。当浸出时间达到 28 d 时,高 CaO 含量样品的LRSi、LRCa和 LRLa分别都小于低 CaO 含量样品的 LRSi、LRCa和 LRLa。这是因为 CaO 含量的增加,玻璃陶瓷样品的硅酸盐氧基磷灰石相强度增强,Si、Ca 和 La 三种元素被很好地固定在了氧基磷灰石晶相的晶格中,不易浸出,具备优异的化学稳定性。14 d 后 LRSi、 LRCa 和 LRLa 分别保持在 2. 0 × 10-3g · m-2 · d-1、1. 5 × 10-3g·m-2·d-1和 2. 5 × 10-5g·m-2·d-1以下,这与大多硼硅酸盐固化体相比具有更好的化学稳定性,体现了硅酸盐氧基磷灰石晶体具有优异的化学稳定性[15,18]。根据浸出结果可知,14 d 后 LRLa比 LRSi、LRCa低两个数量级,这反映了硅酸盐氧基磷灰石晶体对 La 优异的固化能力[37]。由图 8 可知,所有样品的浸出率数据均小于核工业关于固化体化学稳定性浸出率标准值(1 g·m-2·d-1)[38]。综合 28 d 时的 LRSi、LRCa和 LRLa来看,CaO 摩尔分数为 15% 时,制备的玻璃陶瓷样品具有最优异的化学稳定性。
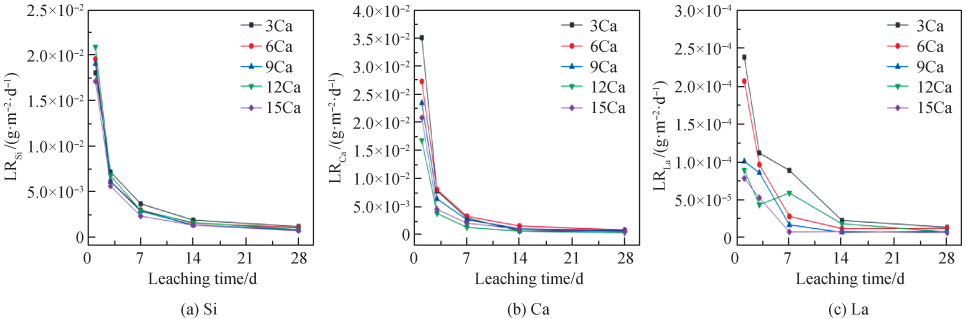
图 8 不同 CaO 含量玻璃陶瓷样品关于 Si、Ca、La 的归一化浸出率
3 结 论
本研究以简化的含 La 和 Ca 的 Na2O-CaO-La2O3-B2O3-SiO2 硼硅酸盐玻璃为基础玻璃,采用二次热处理的方法制备性能优异的氧基磷灰石相玻璃陶瓷,丰富了氧基磷灰石相玻璃陶瓷固化的内容,为富 La 和部分锕系元素的高放废物的固化处理提供了一定的参考价值,通过分析得到了以下结论:
(1)增大 CaO 含量能促进含 La 硅酸盐氧基磷灰石晶相的析出,同时抑制其他晶相的析出;其次,CaO 可以促进硅酸盐氧基磷灰石晶体由 NaLa9(SiO4)6O2 转变为 CaLa4(SiO4)3O,当 CaO 摩尔分数为 15% 时,形成了只含有 CaLa4(SiO4)3O 氧基磷灰石晶相的玻璃陶瓷。
(2)随着 CaO 含量增加,样品的体积密度值呈增大趋势,真实密度呈减小趋势,摩尔体积值呈现减小趋势;CaO 含量会影响陶瓷相中晶体的大小、分布、形状和晶相种类,当 CaO 摩尔分数为 15% 时,析出晶体大小均匀、分布均匀,且 La 元素在玻璃相和陶瓷相都呈均匀分布。
(3)CaO 含量越大,玻璃陶瓷样品的化学稳定性越好;硅酸盐氧基磷灰石相玻璃陶瓷对 La 元素的固化能力比 Si、Ca 两种元素强;14 d 后玻璃陶瓷样品的 LRSi、LRCa和 LRLa分别保持在 2. 0 × 10-3g·m-2·d-1、1. 5 × 10-3g·m-2·d-1和 2. 5 × 10-5g·m-2·d-1以下,具有优异的化学稳定性;CaO 摩尔分数为 15% 时,制备的玻璃陶瓷样品具有最优异的化学稳定性。
参考文献:略
声明:本文由 CERADIR 先进陶瓷在线平台的入驻企业/个人提供或自网络获取,文章内容仅代表作者本人,不代表本网站及 CERADIR 立场,本站不对文章内容真实性、准确性等负责,尤其不对文中产品有关功能性、效果等提供担保。本站提醒读者,文章仅供学习参考,不构成任何投资及应用建议。如需转载,请联系原作者。如涉及作品内容、版权和其它问题,请与我们联系,我们将在第一时间处理!本站拥有对此声明的最终解释权。