摘要: γ-AlON透明陶瓷具有硬度大、化学稳定性好以及光学透过率高等优点,在国防与商业领域具有广阔的应用前景。高纯超细、粒径分布均匀、几乎无团聚的单相γ-AlON粉体是制备高透明γ-AlON陶瓷的关键。本文首先对Al2O3-AlN相图及γ-AlON的热力学计算结果进行了简要介绍,然后综述了高温固相反应、铝热还原氮化、碳热还原氮化三种方法合成γ-AlON粉体的研究进展,最后对粒径小于100 nm的γ-AlON粉体合成方向进行了展望。
关键词: 氮氧化铝, 粉体合成, 高温固相反应, 铝热还原氮化, 碳热还原氮化
0 引 言
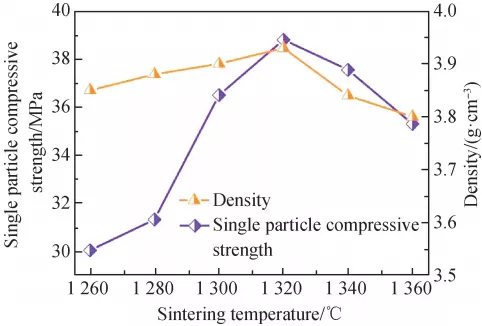
α-Al2O3 是一种常见的综合性能十分优异的结构材料。 然而,因晶体结构对称性较差,制备可见光高透明 α-Al2O3 陶瓷异常困难[1]。1959 年,Yamaguchi 等[2] 发现在 α-Al2O3 中引入少量的氮可促使晶体结构从六方向立方转变形成尖晶石型氮氧化铝 γ-AlON(下文简称 AlON)。与 α-Al2O3 相比,AlON 不仅保留了硬度高、强度大、耐高温和化学稳定性好等优良特性,而且还具有光学各向同性,从而能够制备出综合性能优异的可见-红外光高透明 AlON 陶瓷。自 1979 年 Mccauley 等[3]首次报道 AlON 半透明陶瓷以来,有关 AlON 透明陶瓷的研究在国内外持续受到关注并取得巨大进展[4-5]。通过多年的研究与积累,美国 Surmet 公司已成为全球 AlON 透明陶瓷唯一供货商,生产的 AlON 透明陶瓷可见光透过率已接近理论透过率,平板最大尺寸可达 45. 72 cm × 88. 90 cm(如图 1)[6]。此外,该公司还能够制备复杂形状与折射率渐变的 AlON 透明陶瓷,其产品已成功应用于透明装甲、导弹头罩、红外窗口等国防与商业领域[7-8]。国内有关 AlON 透明陶瓷的研究起步相对较晚,但最近十年仍取得了显著的进步,其中,上海硅酸盐研究所、武汉理工大学、四川大学、大连海事大学、上海大学、福建物质结构研究所、北京中材人工晶体研究院等单位的研究较为系统与深入[5,9-14]。迄今为止,国内上述单位已能够制备出可见光直线透过率超过 80% 的 AlON 透明陶瓷样品,但总体上仍处于实验室阶段[5]。

图 1 Surmet 公司生产的 45. 72 cm × 88. 90 cm AlON® 窗口照片及其直线透过率曲线
为了获得高透明 AlON 陶瓷,通常采用两步法,即先合成 AlON 粉体再高温烧结致密化。 其中,高纯超细、粒径分布均匀、几乎无团聚的单相 AlON 粉体是制备高透明 AlON 陶瓷的关键[15]。目前,合成 AlON 粉体的方法有高温固相反应、铝热还原氮化、碳热还原氮化、高温自蔓延、冲击波等离子体技术、化学气相沉积法、等离子体电弧熔融、肼溶胶-凝胶法等[13,16-22],其中合成 AlON 透明陶瓷粉体以前三种最为常见。而采用这些方法制备单相 AlON 粉体均需满足一定的热力学条件,因此,本文首先简要介绍 Al2O3-AlN 相图及相关热力学计算结果,再分别对高温固相反应、铝热还原氮化、碳热还原氮化这三种合成方法进行综述。
1 Al2O3-AlN 相图与热力学计算
20 世纪 60 年代 Lejus 等[23-24]绘制了第一张 Al2O3-AlN 伪二元系相图,AlON 单相区位于 1 600 ℃ 之上,其中心位于 25% (摩尔分数) AlN 处。在此基础上,Gauckler 等[25] 增加了 AlN 多型体形成区。1979 年McCauley 等[3]绘制出新的 Al2O3-AlN 伪二元系相图,该相图显示 AlON 中心 AlN 含量为 35. 7% (摩尔分数)。1983 年他们进一步完善了该相图,AlON 最低形成温度为 1 700 ℃ ,添加了更多的 AlN 多型体形成区以及高温固/ 气、气/ 液、液/ 固平衡区,并纠正了 AlON 在高温下为一致熔融,这也是迄今为止最为完整的实验相图(如图 2(a))[26]。1992 年 Willems 等[27]通过晶格常数与组成之间的线性关系确定了 AlON 的单相区域,单相区位于 1 640 ℃之上,中心位于 28% (摩尔分数)AlN 处,并发现 AlON 的单相区域随着温度升高而变大,这与 Lejus 等[23-24]的研究一致。2003 年 Nakao 等[28]通过测定 N2 与 CO 的平衡浓度计算出 AlON 的最低形成温度为 1 630 ℃ 。
在实验相图确立的同时,不少研究者开始基于已有的热力学数据,利用不同的热力学模型计算 AlON 的生成自由能,从而获得 AlON Gibbs 反应自由能 ΔGσr 与温度 T 之间的函数关系,并建立了 Al2O3-AlN 计算相图。1979 年 Kaufman[29]和 Dörner[30]等率先进行了相关计算工作,其中 Al7O9N 热力学计算结果分别如下:
ΔGσr = - 515 - 0. 259T (1)
ΔGσr = 1 905 - 1. 017T (2)
前者的计算显示 AlON 从室温到高温一直稳定,而后者的结果表明 1 600 ℃以上 AlON 保持稳定,这与多数实验的结果吻合。1992 年 Willems 等[31]根据 AlON 晶体结构中的空位缺陷重新评估了其熵值,得到 Al23O27N5的生成自由能,并以此计算出 AlON 的最低形成温度为 1 640 ℃ 。1995 年 Dumitrescu 等[32]通过计算获得了较为完整的计算相图,AlON 最低形成温度为 1 612 ℃ ,AlON 的单相区域也是随着温度上升而增大,1997 年Qiu 等[33]计算获得的相图与之非常类似(如图 2(b))。迄今为止,热力学结果与相图(Kaufman[29] 除外)仍存在一些差异,但几乎都表明 Al2O3 与 AlN 反应合成单相 AlON 应在 1 600 ℃以上的高温下进行。
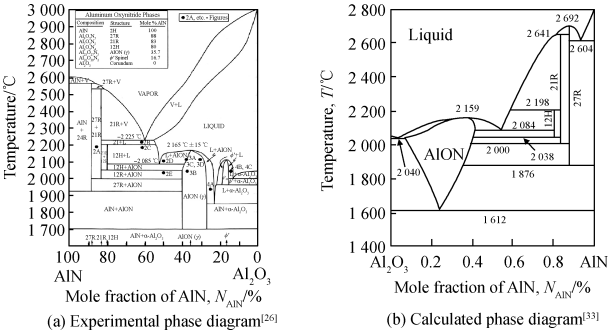
图 2 Al2O3-AlN 的(a)实验相图和(b)计算相图
无论是实验相图还是计算相图,上述相图的建立多以 1 个大气压 N2 为前提。Willems 等[31]通过不同化学反应的热力学数据,绘制了 2 000 K 不同碳活度条件下 Al-O-N 热力学参数状态图。 结果表明:在该温度下 AlON 稳定区间很窄,极易受氮与氧气氛影响而转化成 AlN 或 Al2O3 ,同时碳的活度也对 AlON 稳定区间有一定影响。此后,王习东[34]、王跃忠[35]和 Xie[36]等基于 Willems[31] 和 Dörner[30] 等的研究结果先后利用拟抛物线规则分别对 Al-O-N 热力学参数状态图进行了进一步的研究,发现 AlON 相稳定区范围随温度增加逐渐扩大,受气氛及其分压的影响逐渐变弱。总而言之,为了获得纯相 AlON 粉体,除了满足相应的化学组成外,还需对气氛、温度等合成条件进行严格控制。
2 粉体合成
2. 1 高温固相反应
高温固相法是将氧化铝和氮化铝按一定配比混合,在高于 1 650 ℃ 及氮气气氛下,保温一段时间合成AlON 粉体,反应如下
Al2O3 (s) + AlN(s) → AlON(s) (3)
为了在相对较低的温度下合成适用于制备 AlON 透明陶瓷的高纯粉体,需基于相图选择合适的配比。刘学建等[37]采用高温固相法研究了不同配比对产物相组成的影响,结果表明在 1 800 ℃保温 4 h,当 AlN 含量为 27% ~ 33% (摩尔分数)时,产物中除了少量的 AlN 外,其余均为 AlON,继续增加或降低 AlN 的含量,第二相含量均增加。同时,研究还发现低温下 Al2O3 优先进入 AlON 晶格中形成富氧的 AlON,然后在高温下AlN 进一步固溶形成富氮的 AlON 相,这与 Bandyopadhyay 等[38]的研究结果一致。原料的粒径大小以及缺陷的多少对高温固相反应有重要的影响,采用粒径小、结构疏松、缺陷多的原料有利于促进界面化学反应与离子的扩散,从而降低反应温度与减少保温时间。齐建起等[39-40] 采用粒径均小于 100 nm 的 α-Al2O3 与γ-Al2O3 混合物与微米或纳米 AlN 粉体作为原料,结果表明,采用纳米 AlN 原料活性更高,在 1 750 ℃ 保温4 h 即可合成单相 AlON 粉体。Li 等[16]将粒径为 3 μm 的 AlN 原料首先进行球磨制得缺陷多、活性高的纳米颗粒,再与纳米 Al2O3 球磨,所得的混合粉末在 1 680 ℃仅保温 20 min 即可形成单相 AlON 粉体。提高升温速率能有效抑制升温过程中原料颗粒的长大,从而降低合成温度而获得晶粒细小的产物。孟志民[41]采用高温固相快速合成 AlON 粉体,研究了升温速率对合成的 AlON 粉体相组成与形貌的影响,结果表明,当升温速率为 100 ℃ / min 时可在较低的温度 1 700 ℃合成单相 AlON 粉体,该粉体粒径分布窄,形状近似球形,粒径为 1 ~ 4 μm,几乎不团聚。
尽管高温固相反应法合成简单,工艺过程容易控制且适合大规模生产,但大部分采用高温固相反应法合成后的粉体晶粒粗大、烧结活性低,通常团聚严重需要强力球磨,并且原料 AlN 较贵,导致生产成本升高。此外,AlN 粉体容易水化,在贮存与混料过程中需避免吸潮及与水接触。
2. 2 铝热还原氮化
为了避免使用容易水化且价格相对较高的氮化铝,采用铝热还原氮化法合成 AlON 粉体是一种较好的选择。该法通常以氧化铝和铝粉为原料,在流动的氮气中高温反应生成 AlON 粉体,反应如下:
Al2O3 (s) + Al(s) + N2 (g) → AlON(s) (4)
采用该法在相对较低的温度下合成纯相 AlON 粉体,需要选择合适的铝粉粒径与含量。一方面,铝粉颗粒越小高温非均相反应速率越快,合成温度越低;但另一方面,铝粉颗粒越小表面氧化越严重,化学组成控制越难。周纪承等[42]采用粒径为 20 ~ 30 nm 的 γ-Al2O3 (由硫酸铝铵煅烧制得)和粒径为 1 ~ 2 μm Al 粉合成AlON 粉体,研究铝含量对合成 AlON 粉体的影响,结果表明,当 Al 的含量从 12% (质量分数)降至 10% (质量分数)时,1 800 ℃保温 3 h 可获得单相 AlON 粉体。常见的球磨混料方式容易破坏铝粉表面的氧化层并进一步氧化。Su 等[13]在无保护气氛下采用磁力搅拌的方式进行混料,粒径为 1. 5 μm 球形铝颗粒能保持完好,并较均匀分布在 Al2O3 粉体中,在 1 750 ℃ 氮气条件下保温 3 h 合成纯相 AlON 粉体,AlON 晶粒发育良好,呈多面体形态,粒径为 10 ~ 30 μm。为了降低成本、避免铝粉氧化以及提高粉体的反应活性,Miao 等[43]选择粗颗粒的 Al 粉为原料,与 γ-Al2O3 混合在氮气或氨气保护气氛下进行高能球磨,将所得粒径为 5 ~ 30 nm的纳米混合粉体升至 1 650 ~ 1 700 ℃ 保温即可获得单相 AlON。Al2O3 的粒径与晶型对铝热还原氮化反应也有影响。齐建起等[44-45]发现当采用 γ-Al2O3 为原料时,在 1 700 ℃保温 3 h 即可得到纯相 AlON 粉体,比采用 α-Al2O3 低 50 ℃ ,且球磨后的粉体更均匀细小。 这是因为同样尺寸的纳米 γ-Al2O3 比 α-Al2O3 有更高的稳定性,在更高的温度下才发生粗化,从而保持粉体在高温下的活性[45-46]。气氛的状态同样影响 AlON 粉体的合成。潘磊等[47]发现在流动氮气条件下合成 AlON 粉体温度(1 750 ℃ )比静态氮气的温度(1 800 ℃ )低,而且制得的粉体粒径(2 ~ 5 μm)比静态氮气合成的(5 ~ 8 μm)小,粒度分布更窄,大颗粒也明显减少。这种结果的产生与流动气氛中更高的氧分压以及气流能够带走挥发性的碳有关。
齐建起[48]对铝热还原氮化过程进行了较为详细的描述。即铝粉受热熔化、铝粉氮化生成 AlN 以及 AlN与 Al2O3 固相反应生成 AlON。在生成 AlON 之前,Al 始终处于不稳定状态,要发生向 Al2O3 或 AlN 的转变,这种转变与炉内氧分压有密切关系。而生成 AlON 之后,因 AlON 的稳定区很窄且随温度发生变化,为了维持 AlON 相的稳定性,高温需缓慢升温并保温一定时间。Su 等[13] 也对铝热还原氮化过程进行了研究,发现Al2O3 可以作为稀释剂,能有效阻止铝粉在氮化过程中引起的团聚,从而有利于原位氮化。
铝热还原氮化法原料容易获得、生产成本低、合成后的粉体残碳少,易于获得白色的粉体。但采用该法铝粉在混料等过程中易被氧化,从而导致难以准确控制 AlON 化学组成,同时也存在合成的 AlON 团聚严重或晶粒粗大等缺点。
2. 3 碳热还原氮化
碳热还原氮化法通常以氧化铝和碳粉为原料,经混合后在氮气气氛下碳热还原氮化反应生成 AlON,其反应方程式如式(5)所示。采用该方法原料容易获得且较为廉价,合成成本低,制备的 AlON 粉体具有粒度均匀、粒度小、团聚少等优点。
优点。
Al2O3 (s) + C(s) + N2 (g) → AlON(s) + CO(g) (5)
碳热还原氮化法一般采用两步进行,首先升温至 1 500 ~ 1 600 ℃进行保温一段时间生成 AlN,然后再继续升高温度到 1 700 ℃以上合成 AlON[49-52]。Zheng 等[53]以不同晶型或粒径的氧化铝与炭黑为原料进行配比,在 1 600 ℃保温 1 ~ 2 h,再升温至 1 800 ~ 1 850 ℃保温 1 h,可获得单相 AlON。通过详细的研究与对比,发现在石墨炉中直接升温至 1 750 ℃ 以上容易过度氮化,无法获得纯相 AlON 粉体;而采用两步法通过控制温度、气体压力等参数能够获得粒度分布均匀的纯相 AlON。Xie 等[36] 对两步法做了进一步的研究,发现在1 200 ~ 1 600 ℃保温 2 h,在 1 750 ℃保温 1. 5 h 均可形成单相 AlON,但第一步相对较低的温度易导致 AlON严重团聚,这主要由残留碳诱导的 AlON 气相生长所致。因此,该研究解释了两步碳热合成的第一步其实质是在 1 500 ~ 1 600 ℃通过碳热还原氮化反应生成 AlN,并尽可能促使碳反应完全,从而使得在 1 650 ℃以上AlON 的形成主要通过 Al2O3 和 AlN 固相反应,而不是气相反应。
采用碳热还原氮化法合成 AlON 粉体,需选择合适的 Al2O3 与碳粉。邓启煌等[54]采用 γ-Al2O3 、α-Al2O3和石墨粉体为原料,研究了 Al2O3 晶型对粉体合成的影响,以 γ-Al2O3 为原料在 1 900 ℃合成出分散性较好,颗粒粒径大小在 2 ~ 5 μm 的 AlON 粉体。雷景轩等[55]研究了碳源的结构形态对 AlON 粉体合成的影响,结果发现与微米碳粉相比,纳米碳黑可以降低合成温度,在 1 730 ℃ 即可合成粒径为 2 ~ 5 μm 粉体。许建鑫等[56]研究了形核密度对 AlON 粉体相组成与形貌的影响,结果表明,选用比表面积大的活性炭为原料时形核密度高,易于得到结构疏松、晶粒较小、烧结活性高的 AlON 粉体。
采用不同结晶状态的氧化铝和碳粉为原料,这种传统碳热还原氮化法尽管工艺简单,容易大规模生产,但合成的 AlON 粉体常存在一定程度的团聚且颗粒仍较大,合成温度偏高,这主要源于升温过程中 Al2O3 颗粒之间发生了烧结与粗化[57]。为了避免这种现象,在碳热还原氮化前制备具有核壳结构的前驱体,即在氧化铝的表面形成一层既作为碳源又起隔绝作用的碳膜,是一种行之有效的方法。盛鸿飞等[58]采用葡萄糖和α-Al2O3 作为原料,以无水乙醇为球磨介质球磨混合后热解制得碳包覆 Al2O3 的混合物,在 1 700 ℃保温 1 h即可合成纯相 AlON 粉体。Yuan 等[57]采用一种碳热还原氮化与高温固相反应联合的方法,即先在 γ-Al2O3的表面包覆一层由蔗糖热解成的碳膜,在 1 500 ℃ 碳热还原氮化后所形成的 Al2O3/ AlN 复合粉末再与适量Al2O3 混合,然后在 1 750 ℃ 高温固相反应得到白色的纯相 AlON 粉体,该方法可有效避免碳热还原氮化中的过度氮化。Xie 等[59]以 γ-Al2O3 和蔗糖为原料,以乙醇-水为混合溶剂制备蔗糖包覆的 γ-Al2O3 前驱体,再进一步碳热氮化,通过控制蔗糖与乙醇的含量,得到分散性好、粒径为 0. 6 ~ 1. 0 μm 的 AlON 粉体,其形成示意图如图 3 所示。

图 3 AlON 粉体形成示意图
Jin 等[60]采用 γ-Al2O3 、尿素与甲醛为原料,通过原位聚合法形成核壳结构的 Al2O3/ UFR(脲醛树脂)纳米复合物,结果表明,由 UFR 热解的碳阻碍了 Al2O3 的生长与团聚,在 1 720 ℃ 合成出白色的纯相 AlON 粉体,粉体呈双峰分布(粒径为0. 2 μm 和0. 7 μm),分散性好,将合成的粉末在1 950 ℃下烧结 AlON 透明陶瓷其直线透过率超过 80% 。Deng 等[61] 采用水热法合成了 Al2O3/ C 前驱体,之后通过 SPS(放电等离子体烧结)快速合成,仅在1 680 ℃保温5 min 就合成了粒径为0. 5 ~ 1 μm 的纯相 AlON 粉体。Subaghi 等[62]在室温条件下通过超声波法先合成 γ-Al2O3/ PAN(聚丙烯腈)纳米前驱体,再热解获得 γ-Al2O3/ C 核壳结构,最后通过两步碳热还原氮化法合成粒径约为 0. 6 ~ 0. 75 μm 的单相 AlON 粉体。
相对高温固相反应和铝热还原氮化,碳热还原氮化更加灵活多变,能够合成出粒径更为细小的 AlON 粉体。但是,无论是传统的碳热还原氮化还是形成核壳结构前驱体再进一步碳热氮化,都需仔细控制组成与工艺,避免碳的过多残留以及过度氮化。
3 结 语
综上所述,采用高温固相反应法、铝热还原氮化法和碳热还原氮化法均能合成单相亚微米级 AlON 粉体。将合成的粉体再经球磨细化以及添加适量的烧结助剂可制备出透过率达 80% 及以上的 AlON 透明陶瓷。而无论使用上述哪种方法,原料的粒径、晶型、缺陷以及不同原料的接触状态总是影响 AlON 粉体合成的温度以及合成速率。此外,目前采用上述三种方法合成单相 AlON 温度均需在 1 600 ℃以上,这与相图高度吻合。
然而,以上述三种方法合成的粉体即使经过球磨后,烧结温度仍然较高( > 1 900 ℃ ),这导致晶粒粗大(一般 50 ~ 150 μm)从而严重降低 AlON 陶瓷的强度。采用更为细小的纳米粉体烧结是制备细晶高强透明陶瓷的有效举措。因此,为了获得活性高、杂质少、粒径小于 100 nm 的单相 AlON 粉体,可以尝试使用或改进下面几种合成技术:
(1)继续探索新的湿化学法合成具有 Al2O3/ C 核壳结构的前驱体,在低于 1 700 ℃的条件下快速碳热还原氮化。
(2)采用肼溶胶-凝胶法,使得前驱体内部直接形成部分 Al-N 键,在 AlON 分解动力学条件不充分的温度下通过离子位置的微调节原位合成 AlON 粉体,该方法可大幅降低 AlON 粉体合成温度。
(3)采用化学气相沉积法与等离子体电弧法,前者以高反应活性的卤化铝代替高稳定性的氧化铝为原料,在 1 000 ℃左右即可合成 AlON,而后者获得的粉体呈球形且分散性好。
参考文献:略
声明:本文由 CERADIR 先进陶瓷在线平台的入驻企业/个人提供或自网络获取,文章内容仅代表作者本人,不代表本网站及 CERADIR 立场,本站不对文章内容真实性、准确性等负责,尤其不对文中产品有关功能性、效果等提供担保。本站提醒读者,文章仅供学习参考,不构成任何投资及应用建议。如需转载,请联系原作者。如涉及作品内容、版权和其它问题,请与我们联系,我们将在第一时间处理!本站拥有对此声明的最终解释权。